วันจันทร์ที่ 28 กันยายน พ.ศ. 2563
วันอังคารที่ 8 กันยายน พ.ศ. 2563
ปฏิกิริยาเคมี
การเกิดปฏิกิริยาเคมี
เป็นการเปลี่ยนแปลงของสารที่ได้ผลิตภัณฑ์ของสารที่แตกต่างจากสารเดิมโดยสังเกตจากการเปลี่ยนสีของสาร การเกิดตะกอน หรือการเกิดกลิ่นให้
ปฏิกิริยาเคมี (chemical reaction)
คือ กระบวนการที่เกิดจากการที่สารเคมีเกิดการเปลี่ยนแปลงแล้วส่งผลให้เกิดสาร ใหม่ขึ้นมาซึ่งมีคุณสมบัติเปลี่ยนไปจากเดิม การเกิดปฏิกิริยาเคมีจำเป็นต้องมีสารเคมีตั้งต้น 2 ตัวขึ้นไป (เรียกสารเคมีตั้งต้นเหล่านี้ว่า "สารตั้งต้น" หรือ reactant)ทำปฏิกิริยาต่อกัน และทำให้เกิดการเปลี่ยนแปลงในคุณสมบัติทางเคมี ซึ่งก่อตัวขึ้นมาเป็นสารใหม่ที่เรียกว่า "ผลิตภัณฑ์" (product) ซึ่งสารผลิตภัณฑ์มีคุณสมบัติทางเคมีที่เปลี่ยนไปจากเดิม
หลังจากการเกิดปฏิกิริยาเคมีอะตอมทั้งหมดของสารตั้งต้นไม่มีการสูญหายไปไหนแต่เกิดการแลกเปลี่ยนจากสารหนึ่งไปสู่อีกสารหนึ่ง
ซึ่งจะเห็นได้จากผลรวมของอะตอมของสารตั้งต้นจะเท่ากับผลรวมของอะตอมของผลิตภัณฑ์
ปฏิกิริยาเคมีมีขั้นตอนของการเปลี่ยนแปลงตามลำดับผัง เหตุการณ์ ต่อไปนี้
 ปฏิกิริยาเคมีแบ่งออกได้ 5 ชนิด ได้แก่
ปฏิกิริยาเคมีแบ่งออกได้ 5 ชนิด ได้แก่
1. ปฏิกิริยาการรวมตัว A +Z -------> AZ
2. ปฏิกิริยาการสลายตัว AZ -------> A +Z
3. ปฏิกิริยาการแทนที่เชิงเดี่ยว A + BZ -------> AZ + B
4. ปฏิกิริยาการแทนที่เชิงคู่ AX+BZ -------> AZ + BX
5. ปฏิกิริยาสะเทิน HX+BOH -------> BX + HOH
ข้อสังเกตการเกิดปฏิกิริยาเคมี
สารใหม่ที่เกิดขึ้นในปฏิกิริยาเคมี สังเกตได้ดังนี้
1. สี เช่น สารเดิมไม่มีสีเมื่อเกิดปฏิกิริยาเคมี จะมีสีใหม่เกิดขึ้น (สารใหม่)
2. กลิ่น เช่น เกิดกลิ่นฉุน กลิ่นเหม็น กลิ่นหอม
3. ตะกอน เช่น สารละลายเลด (II) ไนเตรต และโพแทสเซียมไอโอไดด์ เป็นของเหลวใส ไม่มีสี เมื่อผสมกันแล้วเกิดตะกอนสีเหลือง
4. ฟองแก๊ส เช่น กรดไฮโดรคลอริก ผสมกับหินปูนหรือแคลเซียมคาร์บอเนตเกิดฟองแก๊สขึ้น
5. เกิดการระเบิด หรือเกิดประกายไฟ เช่น ใส่โลหะโซเดียมลงในน้ำจะเกิดประกายไฟขึ้น
6. มีอุณหภูมิเปลี่ยน ซึ่งสารโดยทั่วไปเมื่อเกิดปฏิกิริยาเคมีจะเกิดการเปลี่ยนแปลง พลังงาน ความร้อนควบคู่ไปด้วยเสมอ
พลังงานกับการเกิดปฏิกิริยา
พลังงานเคมี (Chemical energy)เป็นพลังงานศักย์ที่แฝงอยู่ในโครงสร้างของสาร เช่นอยู่ในรูปของน้ำมันเชื้อเพลิงไขมัน
ซึ่งเมื่อเกิดการเผาไหม้จะปล่อยพลังงานเคมีออกมา
และนำมาใช้ประโยชน์ได้พลังงานเคมีเป็นพลังงานที่มีส่วนเกี่ยวข้องและสำคัญกับสิ่งมีชีวิตมาก
ในการเกิดปฏิกิริยาของสารแต่ละปฏิกิริยานั้นต้องมีพลังงานเข้ามาเกี่ยวข้องกับการเกิดปฏิกิริยาเคมี 2 ขั้นตอนดังนี้
ขั้นที่ 1 เป็นขั้นที่ดูดพลังงานเข้าไปเพื่อสลายพันธะในสารตั้งต้น
ขั้นที่ 2 เป็นขั้นที่คายพลังงานออกมาเมื่อมีการสร้างพันธะในผลิตภัณฑ์
1.ปฏิกิริยาดูดความร้อน (Endothermic reaction)
เป็นปฏิกิริยาที่ดูดพลังงานเข้าไปสลายพันธะมากกว่าที่คายออกมา
เพื่อสร้างพันธะ โดยในปฏิกิริยาดูดความร้อนนี้สารตั้งต้นจะมีพลังงานต่ำกว่าผลิตภัณฑ์จึงทำให้สิ่งแวดล้อมเย็นลง
อุณหภูมิลดลง เมื่อเอามือสัมผัสภาชนะจะรู้สึกเย็นดังภาพ
2.ปฏิกิริยาคายความร้อน ( Exothermic reaction)
เป็นปฏิกิริยาที่ดูดพลังงานเข้าไปสลายพันธะน้อยกว่าที่คายออกมาเพื่อสร้างพันธะ โดยในปฏิกิริยาคายความร้อนนี้สารตั้งต้นจะมีพลังงานสูงกว่าผลิตภัณฑ์จึงให้พลังงานความร้อนออกมาสู่สิ่งแวดล้อมทำให้อุณหภูมิสูงขึ้นเมื่อเอามือสัมผัสภาชนะจะรู้สึกร้อนดังภาพ
อัตราการเกิดปฏิกิริยาเคมี
อัตราการเกิดปฏิกิริยาเคมีหมายถึงปริมาณสารตั้งต้นที่หายไปต่อหนึ่งหน่วยเวลาหรือปริมาณผลิตภัณฑ์ที่เกิดขึ้นต่อหนึ่งหน่วยเวลา
เมื่อพิจารณาจากปฏิกิริยาต่อไปนี้
A + 2B -------------> C ………..(1)
ในขณะที่ปฏิกิริยาดำเนินไป สาร A และสาร B เป็นสารตั้งต้นถูกใช้ไปดังนั้นความเข้มข้นของสาร A และ B จะลดลงส่วนความเข้มข้นของสาร C ซึ่งเป็นผลิตภัณฑ์จะเพิ่มขึ้น จากปฏิกิริยา (1) จะพบว่าอัตราการลดลงของสาร A เป็นครึ่งหนึ่งของการลดลงของสาร B
ดังนั้นเมื่อเขียนความสัมพันธ์ระหว่างอัตราการเกิดปฏิกิริยาในรูปของสารต่างๆจะต้องคิดต่อ 1 โมลของสารนั้น ซึ่งสามารถเขียนได้ดังนี้
อัตราการเกิดปฏิกิริยาเคมี = ปริมาณของสารตั้งต้นที่ลดลง/เวลา
= ปริมาณของสารผลิตภัณฑ์ที่เกิดขึ้น / เวลา
อัตราเร็วเฉลี่ยหมายถึง อัตราเร็วโดยเฉลี่ย ตั้งแต่เริ่มต้น จนปฏิกิริยาเกิดขึ้นในช่วงเวลาหนึ่ง เช่น อัตราเร็วเฉลี่ยในช่วง 10 วินาที ( หาได้จากการทดลอง)
อัตราเร็ว ณ เวลาหนึ่ง หมายถึง อัตราเร็วของปฏิกิริยาที่ตำแหน่งใดตำแหน่งหนึ่ง เช่น อัตราเร็ว ณ 10 วินาที ( หาจากค่าความชันของกราฟระหว่างปริมาณสารกับเวลา)
ปัจจัยที่มีผลต่ออัตราการเกิดปฏิกิริยา
1. ความเข้มข้นของสารตั้งต้น กรณีที่สารตั้งต้นเป็นสารละลาย ถ้าสารตั้งต้นมีความเข้มข้นมากจะเกิดเร็วเนื่องจากตัวถูกละลายมีโอกาสชนกันมากขึ้นบ่อยขึ้น ในทางตรงกันข้ามถ้าเราเพิ่มปริมาตรของสารละลายโดยความเข้มข้นเท่าเดิมอัตราการเกิดปฏิกิริยาจะเท่าเดิม
2. พื้นที่ผิวสัมผัสกรณีที่สารตั้งต้นมีสถานะเป็นของแข็งสารที่มีพื้นที่ผิวสัมผัสมากจะทำปฏิกิริยาได้เร็วขึ้น เนื่องจากสัมผัสกันมากขึ้น ใช้พิจารณากรณีที่สารตั้งต้นมีสถานะของแข็ง ดังภาพ
ความแตกต่างของ พื้นที่ผิว
3. ความดันกรณีที่สารตั้งต้นมีสถานะเป็นก๊าซถ้าความดันมากปริมาตรก็ลดลง และปฏิกิริยาก็จะเกิดได้เร็วเนื่องจากอนุภาคของสารมีโอกาสชนกันมากขึ้นบ่อยขึ้นในพื้นที่ที่จำกัดนั่นเองดังภาพ
4. อุณหภูมิการที่อุณหภูมิของสารตั้งต้นเพิ่มขึ้นอัตราการเกิดปฏิกิริยาจะเพิ่มขึ้นเนื่องจากเมื่ออุณหภูมิสูงขึ้นโมเลกุลของสารในระบบจะมีพลังงานจลน์สูงขึ้นและมีการชนกันของโมเลกุลมากขึ้น
ปฏิกิริยาที่อุณหภูมิต่ำ ปฏิกิริยาที่อุณหภูมิสูง
5. ตัวเร่งปฏิกิริยา(Catalyst) หมายถึงสารเคมีที่ช่วยทำให้อัตราการเกิดปฏิกิริยาเร็วขึ้นเนื่องจากตัวเร่งจะช่วยในการลดพลังงานกระตุ้นโดยช่วยปรับกลไกในการเกิดปฏิกิริยาให้เหมาะสมกว่าเดิม โดยจะเข้าไปช่วยตั้งแต่เริ่มปฏิกิริยาแต่เมื่อสิ้นสุดปฏิกิริยาจะกลับมาเป็นสารเดิม
6. ธรรมชาติของสาร เนื่องจากสารมีแรงยึดเหนี่ยวซึ่งแตกต่างกันโดยปกติสารประกอบไอออนิกจะเคลื่อนที่ได้เร็วกว่าสารประกอบโควาเลนต์
การจัดอิเล็กตรอนในระดับพลังงาน
__________อิเล็กตรอนในอะตอมที่อยู่ ณ ระดับพลังงาน (energy levels หรือ shell) จะมีพลังงานจำนวนหนึ่ง ส้าหรับอิเล็กตรอนที่อยู่ใกล้นิวเคลียสมากที่สุดจะมีพลังงานน้อยกว่าพวกที่อยู่ไกลออกไป ยิ่งอยู่ไกลมากยิ่งมีพลังงานมากขึ้น โดยกำหนดระดับพลังงานหลักให้เป็น n ซึ่ง n เป็นจ้านวนเต็มคือ 1, 2, … หรือตัวอักษรเรียงกันดังนี้ คือ K, L, M, N, O, P, Q ตามล้าดับ เมื่อ n = 1 จะเป็นระดับพลังงานต่ำสุด หมายความว่า จะต้องใช้พลังงานมากที่สุดที่จะดึงเอาอิเล็กตรอนนั้นออกจากอะตอมได้ จำนวนอิเล็กตรอนที่จะมีได้ในแต่ละระดับพลังงานหลักต้องเท่ากับหรือไม่เกิน 2n2 และจำนวนอิเล็กตรอนในระดับนอกสุดจะต้องไม่เกิน 8 เช่น
____๘ระดับพลังงานที่หนึ่ง n = 1 (shell K) ปริมาณอิเล็กตรอนที่ควรมีอยู่ = 2(1)2 = 2
____๘ระดับพลังงานที่สอง (n = 2) ปริมาณอิเล็กตรอนสูงสุดที่ควรมีได้ = 2(2)2 = 8
____๘ระดับพลังงานที่สาม (n = 3) ปริมาณอิเล็กตรอนสูงสุดที่ควรมีได้ = 2(3)2 = 18
____๘ระดับพลังงานที่สี่ (n = 4) ปริมาณอิเล็กตรอนสูงสุดที่ควรมีได้ = 2(4)2 = 32
____๘ระดับพลังงานที่ห้า (n = 5) ปริมาณอิเล็กตรอนสูงสุดที่ควรมีได้ = 2(5)2 = 50
____๘ระดับพลังงานที่หก (n = 6) ปริมาณอิเล็กตรอนสูงสุดที่ควรมีได้ = 2(6)2 = 72
____๘ระดับพลังงานที่เจ็ด (n = 7) ปริมาณอิเล็กตรอนสูงสุดที่ควรมีได้ = 2(7)2 = 98

ช่น ตารางที่ 1.1 การจัดเรียงอิเล็กตรอนในระดับพลังงานหลักของธาตุต่างๆ

จากการศึกษาสเปกตรัมของธาตุต่างๆ พบว่าในระดับพลังงานหลัก (n) ยังประกอบด้วยระดับพลังงานย่อยหรือเรียกว่า ซับเซลล์ (sub-levels หรือ sub-shells) โดยก้าหนดเป็นสัญลักษณ์คือ s p d และ f ซึ่งในแต่ละระดับพลังงานย่อยจะมีอิเล็กตรอนได้ไม่เท่ากันและมีพลังงานไม่เท่ากัน กล่าวคือ ระดับพลังงานย่อย s มีพลังงานต่ำกว่า p ต่ำกว่า d ต่ำกว่า f ตามล้าดับ ในระดับพลังงานย่อยยังประกอบด้วยออร์บิทัล (orbital) ซึ่งในแต่ละออร์บิทัลมีอิเล็กตรอนได้ไม่เกิน 2 อิเล็กตรอน ดังนี้
____๘๘๘๘ระดับพลังงานย่อย s มีอิเล็กตรอนได้ไม่เกิน 2 อิเล็กตรอน มี 1 ออร์บิทัล
____๘๘๘๘ระดับพลังงานย่อย p มีอิเล็กตรอนได้ไม่เกิน 6 อิเล็กตรอน มี 3 ออร์บิทัล
____๘๘๘๘ระดับพลังงานย่อย d มีอิเล็กตรอนได้ไม่เกิน 10 อิเล็กตรอน มี 5 ออร์บิทัล
____๘๘๘๘ระดับพลังงานย่อย f มีอิเล็กตรอนได้ไม่เกิน 14 อิเล็กตรอน มี 7 ออร์บิทัล
__________ภายในระดับพลังงานหลักอันเดียวกันจะประกอบด้วยพลังงานย่อยเรียงล้าดับจากพลังงานต่้าไปสูง คือ จาก s ไป p d และ f เช่น 3p สูงกว่า 3s ซึ่งเมื่อนำมาเรียงลำดับกันแล้ว พบว่ามีเฉพาะ 2 ระดับพลังงานแรกคือ n = 1 และ n = 2 เท่านั้น ที่มีพลังงานเรียงลำดับกัน แต่พอขึ้นระดับพลังงาน n = 3 เริ่มมีการซ้อนเกยกันของระดับพลังงานย่อย ดังรูป

จากการศึกษาพบว่ากรณีของอะตอมที่มีหลายอิเล็กตรอนนั้นระดับพลังงานของ 3d จะใกล้กับ 4s มาก และพบว่า ถ้าบรรจุอิเล็กตรอนใน 4s ก่อน 3d พลังงานรวมของอะตอมจะต่ำ และอะตอมจะเสถียรกว่า ดังนั้นในการจัดเรียงอิเล็กตรอนในออร์บิทัลแบบที่เสถียรที่สุด คือการจัดตามระดับพลังงานที่ต่ำที่สุดก่อนทั้งในระดับพลังงานหลักและย่อย ซึ่งวิธีการจัดอิเล็กตรอนสามารถพิจารณาตามลูกศรในรูปที่ 1.8 โดยเรียงลำดับได้เป็น 1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d 6p 7s 5f 6d 7p

ในการจัดอิเล็กตรอนอาจเขียนเป็นแผนภาพออร์บิทัลซึ่งแสดงสปินของอิเล็กตรอนด้วย ดังตัวอย่าง C มี z = 6 มีโครงแบบอิเล็กตรอนเป็น 1s2 2s2 2p2 ซึ่งการจัดแสดงสปินของอิเล็กตรอนแสดงในตารางที่ 1.1
__________ในการบรรจุอิเล็กตรอนหรือการจัดเรียงอิเล็กตรอนลงในออร์บิทัลจะต้องยึดหลักในการบรรจุอิเล็กตรอนของอะตอมหนึ่งๆ ลงในออร์บิทัลที่เหมาะสมตามหลักดังต่อไปนี้
__________1) หลักของเพาลี (Pauli exclusion principle) กล่าวว่า “ไม่มีอิเล็กตรอนคู่หนึ่งคู่ใดในอะตอมที่มีเลขควอนตัมทั้งสี่เหมือนกันทุกประการ” นั่นคืออิเล็กตรอนคู่หนึ่งในออร์บิทัลจะมีค่า n, ℓ, mℓ เหมือนกันได้ แต่ต่างกันที่สปิน
__________2) หลักของเอาฟ์บาว (Aufbau principle) มีวิธีการดังนี้
____________๘2.1) สัญลักษณ์วงกลม O, หรือ _ แทน ออร์บิทัล
______________๘๘ลูกศร ↑↓ แทน อิเล็กตรอน 1 ตัว ที่สปิน ขึ้น-ลง
______________๘๘↑↓ เรียกว่า อิเล็กตรอนคู่ (paired electron)
______________๘๘↑ เรียกว่าอิเล็กตรอนเดี่ยว (single electron)
____________๘2.2) บรรจุอิเล็กตรอนเข้าไปในออร์บิทัลที่มีระดับพลังงานต่ำจนครบจำนวนก่อน ดังรูปที่ 1.1
__________3) กฎของฮุนด์ (Hund’s rule) กล่าวว่า “การบรรจุอิเล็กตรอนในออร์บิทัลที่มีระดับพลังงานเท่ากัน (degenerate orbital) จะบรรจุในลักษณะที่ท้าให้มีอิเล็กตรอนเดี่ยวมากที่สุดเท่าที่จะมากได้” ออร์บิทัลที่มีระดับพลังงานมากกว่า 1 เช่น ออรฺบิทัล p และ d เป็นต้น
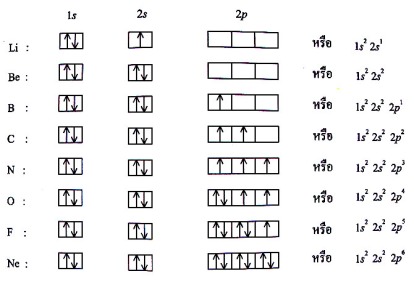
4) การบรรจุเต็ม (filled configuration) เป็นการบรรจุอิเล็กตรอนในออร์บิทัลที่มีระดับพลังงานเท่ากัน แบบเต็ม ครบ 2 ตัว ส่วนการบรรจุครึ่ง (half- filled configuration) เป็นการบรรจุอิเล็กตรอนลงในออร์บิทัลแบบครึ่งหรือเพียง 1 ตัว เท่านั้น ซึ่งการบรรจุทั้งสองแบบ (ของเวเลนซ์อิเล็กตรอน) จะทำให้มีความเสถียรมากกว่าตัวอย่างการบรรจุเต็ม เช่น

ตัวอย่างการจัดอิเล็กตรอนของธาตุเลขอะตอม 1 ถึง 18

วันจันทร์ที่ 7 กันยายน พ.ศ. 2563
-
_ _________ อิเล็กตรอนในอะตอมที่อยู่ ณ ระดับพลังงาน (energy levels หรือ shell) จะมีพลังงานจำนวนหนึ่ง ส้าหรับอิเล็กตรอนที่อยู่ใกล้นิวเคลียสมา...
-
การเกิดปฏิกิริยาเคมี เป็นการเปลี่ยนแปลงของสารที่ได้ผลิตภัณฑ์ของสารที่แตกต่างจากสารเดิมโดยสังเกตจากการเปลี่ยนสีของสาร การเกิดตะกอน หรือการเกิ...










